티스토리 뷰
보령(003850)은 1963년 설립, 1988년 코스피 상장되어 자본금 34,345,000,000원, 보통주 68,690,000주를
코스피시장에서 거래 중에 있다고 소개되어 있습니다.
주요 사업
- 전문, 일반의약품 제조, 매매와 소분, 의약부외품 등의 제조 매매, 생명공학 관련 제품 제공
- 자체 신약 카나브를 다양한 제품, 상품군으로 하여 만성질환군에서 시장점유율 확대 중
개요

전망
- 제약산업의 특성이 첨단 부가가치 산업으로 신약개발 등으로 고수익을 창출할 수 있는 미래 성장 산업이며 다른 산업군에 비해 수요 탄력성이 낮아 경제 흐름의 영향을 덜 받는 특성이 있다고 합니다.
- 정부도 바이오신약, 장기부문을 차세대 10대 성장동력 산업으로 선정 연구기반 조성을 위한 투자 확대 중이어서 제약군의 전망이 있을 것으로 보고 있습니다.
- 고령화 추세로 의약품 시장의 성장성은 지속되며 원천기술 바탕으로 해외시장 진출 노력을 하고 있다고 합니다.
최근의 기사 내용
- 고혈압 3제 복합제 듀카브 플러스 발매 출시 예정
- 보령제약 관계사 바이젠셀 100% 무상증자 결정
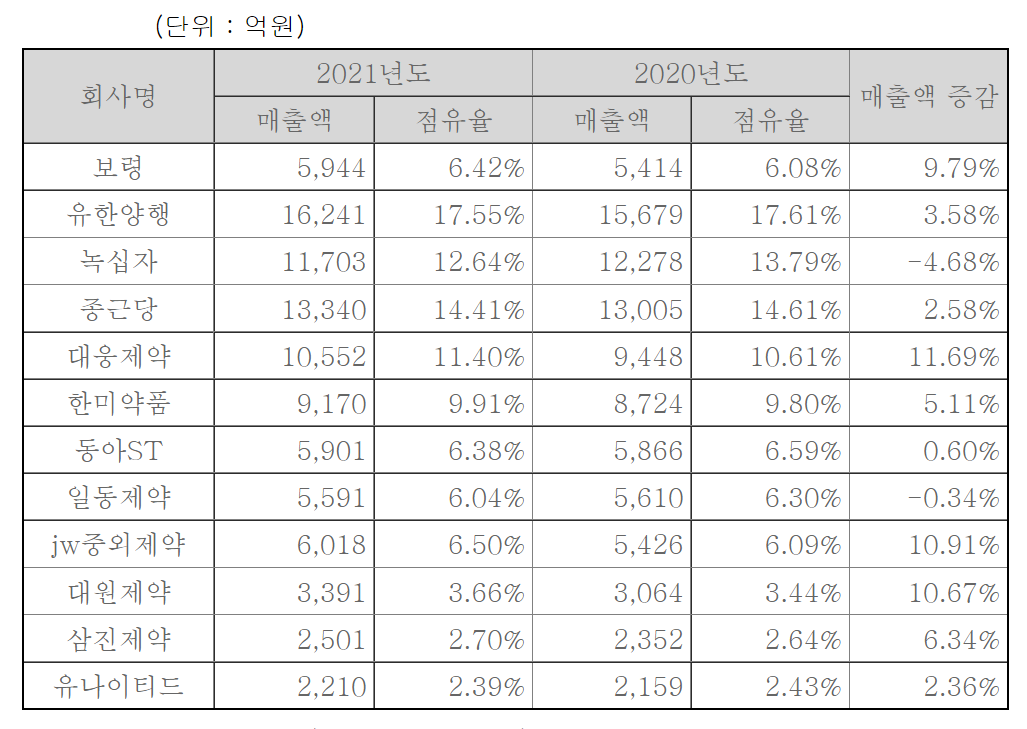
참고로 중요한 내용은 아니지만 제약회사들의 시장점유율입니다.
주목할 만한 내용 공시
투자 판단 관련 주요 경영사항 공시가 26일에 나왔는데요 내용을 이러합니다.
고혈압 개량신약 복합제 BR1015의 한국 식약처(MFDS) 임상 3상 시험계획 승인 신청
그리고 이 사항의 투자 유의 사항이 있었는데요
임상시험 약품이 최종 허가받을 확률은 약 10%이며 임상과정 중 변경 포기할 수도 있다는 내용이 있습니다.
1) 임상시험 제목:
Fimasartan 30mg 단일요법에 적절히 반응하지 않는 본태성 고혈압 환자를 대상으로 Fimasartan 단일요법과 BR1015 병용요법의 혈압 강하 효과와 안전성을 비교하기 위한 무작위 배정, 이중 눈가림, 다기관, 제3상 임상시험
2) 임상시험 단계: 3상
3) 대상질환명(적응증): 고혈압
4) 임상시험 신청(승인) 일 및 승인(시험) 기관:
2022.05.25, 식품의약품 안전처(한국)
5) 임상시험 등록번호:
접수번호 - 20220090983
* 임상시험계획 일련번호는 식약처 승인 후 발급 예정
6) 임상시험의 목적:
Fimasartan 30mg 단일요법에 반응하지 않는 본태성 고혈압 환자를 대상으로 BR1015 병용요법을 Fimasartan 단일요법과 비교하여 8주 후 혈압강하 효과가 우월함을 확인하고, 안전성을 비교 평가한다.
7) 임상시험 시행 방법:
국내 약 244명의 고혈압 환자를 대상으로 약 30개월 동안 진행하는 무작위 배정, 이중 눈가림, 평행, 다기관, 치료적 확증 임상시험(3상)
8) 기대효과:
피마사르탄칼륨 단일요법에 적절히 반응하지 않는 본태성 고혈압 환자에서 피마사르탄칼륨·인다파미드(ARB+티아지드 유사 이뇨제) 병용투여에 대한 유효성 및 안전성을 평가하여 복약순응도 향상 목적의 개량신약 복합제를 개발
9) 기타 사항:
2026년 출시 계획
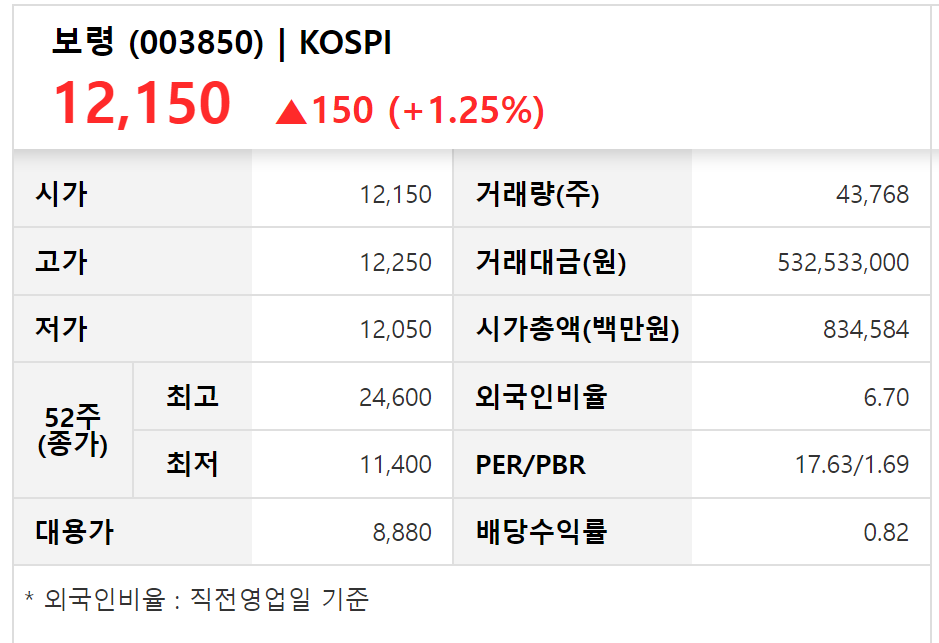
5월 27일 장중 상황이며 52주 최고가가 24600원, 최저가가 11400원입니다.
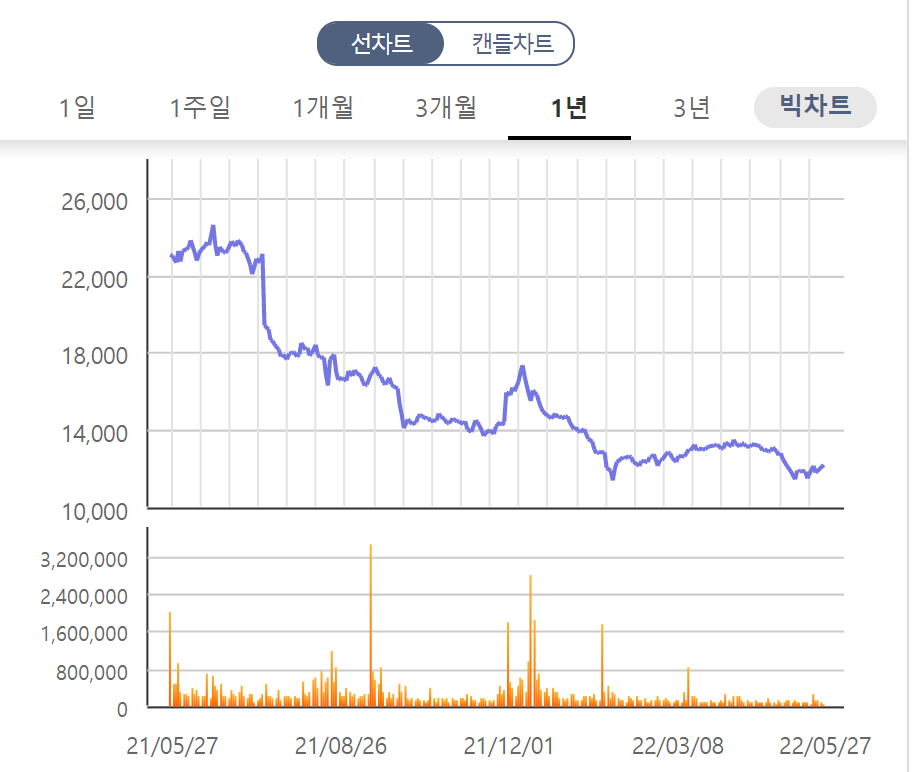
1년 차트입니다.
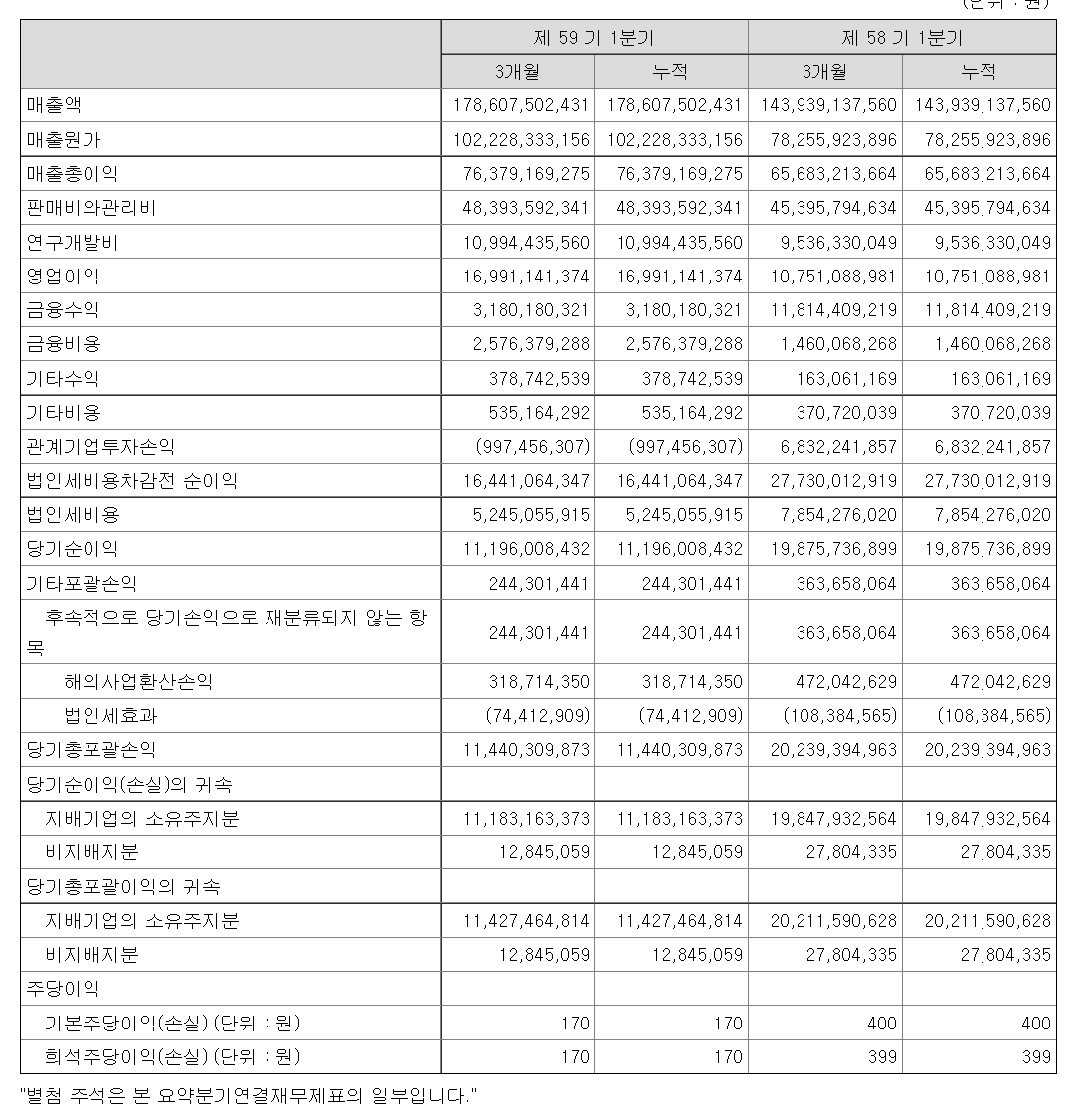
5월에 발표된 분기보고서 중에서 연결 포괄손익계산서입니다.